臨床腫瘍生物学研究室

研究室紹介
臨床腫瘍生物学研究室は、遺伝子診断技術の開発研究を進めていた旧腫瘍ゲノム研究室とオルガノイド培養技術を応用したがん研究を推進する精密腫瘍モデル研究室を母体とし、2026年4月に開設されました。
研究室名に掲げるように、がん専門病院に付設である利点(臨床材料・臨床情報へのアクセス)を活用した「がん」の性状を解き明かす研究を展開することで、私たちはがん医療への貢献を目指します。また、患者由来試料および情報を保管するバイオバンク事業の運営にも尽力し、広範な医学研究のための研究資源の充実と発展を図ります。
構成メンバー
| 室長 | 下里 修 |
|---|---|
| 会計年度任用職員 | 4名 |
プロジェクト紹介
(1) ゲノムコホート研究から見出されたがん関連遺伝子多型の機能解析
がんの早期診断・早期治療は、がんを克服するために最も有効な手段であると考えられます。そのため、がんの高リスク群を層別化し早期治療へとつなげる「先制医療」の実装が期待されています。しかし、その実用化には疾患発症リスクを高い精度で予測するマーカーの発掘が最重要課題といえます。
この課題解決に向けて私たちは、予防疫学研究部と共同してゲノムコホート研究を展開し、遺伝子多型(SNP)に着目してがんの発症リスクを予測することができるか検討しています(図1)。さらに、これらのSNPが持つ機能や発がんへの影響を細胞株や遺伝子改変動物を使って解析しています。
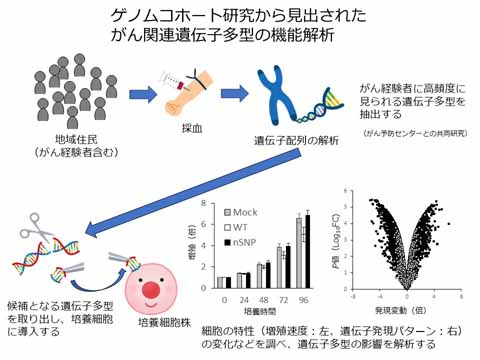
図1 ゲノムコホート研究から見出されたがん関連遺伝子多型の機能解析
地域住民から採取した核酸の塩基配列を読み取り、がん経験者に多く認められる複数の遺伝子多型を見出してきた。様々な手法を用いて、これらががん病態に及ぼす影響を検討している。
(2) 診療と研究をつなぐバイオバンクの進化
患者一人ひとりに最適ながん医療を実現するためには、実際の患者から得られる試料と臨床情報を体系的に管理・提供する研究基盤(バイオバンク)の構築が不可欠です。当センターではこれまで20年以上にわたり、診療後に生じた血清や凍結組織などの残余試料と臨床情報を収集・保管し、研究に提供してきました。この長年の蓄積は、多くの研究を支える重要な基盤となっています。
一方で、上記の保存試料を用いた研究には一定の限界があり、より生体に近い状態での解析が求められています。近年では、生きたがん組織の維持や初代培養細胞の樹立、病理検体を用いた高精度解析が可能となり、これらを新たな研究資源として活用する動きが広がっています。
こうした進展を背景に、当センターでは従来の保存試料に加え、生きたがん組織や細胞、病理検体までを統合的に扱う「次世代型バイオバンク」が構想されています(図2)。
長年にわたり病院バイオバンク管理室と一体となって運営してきた経験を活かし、私たちはこの新たな研究基盤の構築とそれを活用した臨床研究を推進します。診療と研究をつなぐこの取り組みにより、より実践的ながん医療の発展を目指します。
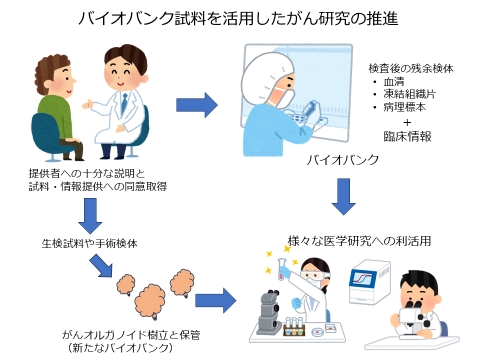
図2 次世代型バイオバンクを活用したがん研究の推進
従来の血液や凍結組織に加え(上段)、生きたがん組織・細胞や病理検体を統合的に収集・管理することで、より生体に近い状態での解析を可能にする(下段)。
業績
-
Shimozato O, Akao N, Yanagisawa Y, Mori Y, Zhang X, Kida Y, Igarashi R, Watanabe T, Ozaki T, Takatori A. Targeting Wnt/β-catenin pathway by DNA alkylating pyrrole-imidazole polyamide in colon cancer. Cancer Science. 117(1): 203-215 (2026)
-
Mori Y, Takeuchi A, Miyagawa K, Yoda H, Soda H, Nabeya Y, Watanabe N, Ozaki T, Shimozato O. CD133 prevents colon cancer cell death induced by serum deprivation through activation of Akt-mediated protein synthesis and inhibition of apoptosis. FEBS Open Bio. 11(5): 1382-1394 (2021)
-
Matsushita M, Mori, Y, Uchiumi K, Ogata T, Nakamura M, Yoda H, Soda H, Takiguchi, N, Nabeya Y, Shimozato O, Ozaki, T. PTPRK suppresses progression and chemo-resistance of colon cancer cells via direct inhibition of pro-oncogenic CD133. FEBS Open Bio. 9(5): 935-346 (2019)
-
Shimozato O, Waraya M, Nakashima K, Souda H, Takiguchi N, Yamamoto H, Takenobu H, Uehara H, Ikeda E, Matsushita S, Kubo N, Nakagawara A, Ozaki T, Kamijo T. Receptor-type protein tyrosine phosphatase kappa directly dephosphorylates CD133 and regulates downstream AKT activation. Oncogene. 34 (15): 1949-1960 (2015)